Reaksi alkilasi pada senyawa karbonil
Alkilasi (Bahasa Inggris: alkylation) atauGugus alkil merupakan gugus univalen yang diperoleh dari alkana yang telah diambil satu atom hidrogen. Dalam Literatur lain, Alkilasi merupakan penambahan jumlah atom dalam molekul menjadi molekul yang lebih panjang dan bercabang. Dalam proses ini menggunakan katalis asam kuat sepertiH2SO4, HCl, AlCl3 (Asam kuat Lewis). Reaksi secara umum adalah sebagai berikut:
RH + CH2=CR’R’’ ---------> R-CH2-CHR’R”
Salah satu reaksi yang paling penting dari enolat adalah alkilasi oleh adanya perlakuan dengan alkil halida. Reaksi ini sangat berguna untuk tujuan sintesis karena memungkinkan pembentukan ikatan karbon-karbon baru, yaitu menggabungkan dua senyawa yang lebih kecil menjadi molekul yang lebih besar. Alkilasi terjadi bila anion enolat yang nukleofilik bereaksi dengan alkil halida yang elektrofilik dan memaksa keluar ‘leaving group’ melalui mekanisme SN2. Reaksi dapat terjadi pada atom oksigen enolat atau karbon alfa, tetapi secara normal terjadi pada atom karbon.
Kedua sintesis yang dibahas dalam bagian ini menyediakan rute ke berbagai macam asam karboksilat dan metil keton. Anda mungkin ingin meninjau faktor-faktor yang mempengaruhi reaksi SN 2 (Bagian 11.3) dalam hubungannya dengan bagian ini.
Anda harus mencoba untuk menghafal struktur ester malonik dan etil asetoasetat. Nama IUPAC dari senyawa ini ditunjukkan pada tabel di bawah ini.
| Struktur | Nama yang umum | Nama IUPAC |
|---|---|---|
 | asam malonat | asam propanedioic |
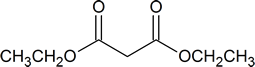 | ester malonis atau dietil malonat | dietil propanedioate |
 | asam acetoacetic | Asam 3-oksobutanoat |
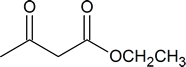 | etil asetoasetat atau ester acetoacetic | etil 3 ‑ oxobutanoate |
Enolat dapat bertindak sebagai nukleofil dalam reaksi tipe S N 2. Keseluruhan hidrogen α diganti dengan gugus alkil. Reaksi ini adalah salah satu yang lebih penting untuk enolat karena ikatan karbon-karbon terbentuk. Alkilasi ini dipengaruhi oleh keterbatasan yang sama seperti reaksi S N 2 yang telah dibahas sebelumnya. Kelompok meninggalkan yang baik, X = klorida, bromida, iodida, tosilat, harus digunakan.Juga, kelompok cuti sekunder dan tersier tidak boleh digunakan karena reaktivitas yang buruk dan kemungkinan persaingan dengan reaksi eliminasi.Terakhir, penting untuk menggunakan basa kuat, seperti LDA atau natrium amida, untuk reaksi ini.Menggunakan basis yang lebih lemah seperti hidroksida atau alkoksida meninggalkan kemungkinan terjadinya beberapa alkilasi.
Sintesis Ester Malotis
Malon ester adalah reagen khusus yang digunakan dalam reaksi yang mengubah alkil halida menjadi asam karboksilat yang disebut Sintesis Ester Malotis.Sintesis ester malonik adalah prosedur sintetik yang digunakan untuk mengubah senyawa yang memiliki rumus struktur umum 1 menjadi asam karboksilat yang memiliki rumus struktur umum 2.

Karena kenyataan bahwa α hidrogen Malonic ester berdekatan dengan dua karbonil, mereka dapat dideprotonasi oleh natrium etoksida (NaOEt) untuk membentuk Sodio Malonic Ester.

Karena Sodio Malonic Ester adalah enolate, maka dapat dialkilasi dengan alkil halida.
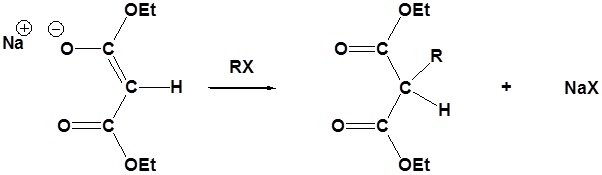
Setelah alkilasi produk dapat diubah menjadi asam dikarboksilat melalui saponifikasi dan selanjutnya salah satu asam karboksilat dapat dihilangkan melalui langkah dekarboksilasi.
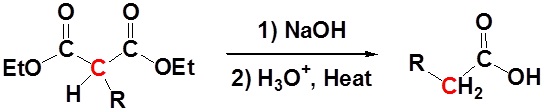
Mekanisme
1) Saponifikasi
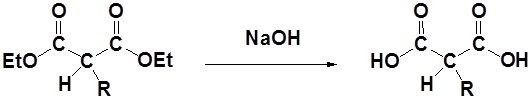
2) Dekarboksilasi
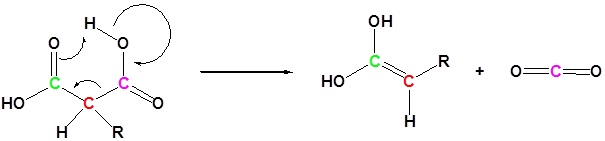
3) Tautomerisasi

Semua langkah bersama membentuk sintesis ester Malison.
\ [RX \ rightarrow RCH_2CO_2H \]
Contoh
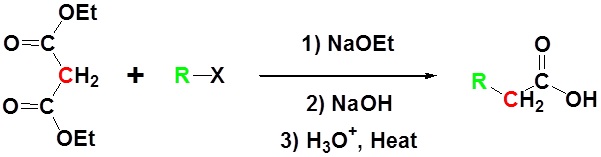
Sintesis Ester Acetoacetic
Sintesis ester asetasetetik memungkinkan konversi etil asetoasetat menjadi metil keton dengan satu atau dua gugus alkil pada karbon alfa.
Tangga
1) Deprotonasi dengan etoksida
2) Reaksi Alkilasi melalui dan SN2
3) Hidrolisis dan dekarboksilasi
Selain kelompok alky kedua
Setelah langkah pertama dan gugus alkil tambahan dapat ditambahkan sebelum tahap dekarboksilasi.Secara keseluruhan ini memungkinkan untuk penambahan dua gugus alkil yang berbeda.
Alkilasi langsung
Sintesis ester malonik dan sintesis ester asetoasetat dapat dibentuk sebelumnya dengan basa yang relatif ringan, seperti natrium etoksida, karena sifat asam yang luar biasa dari senyawa dikarbonil. Namun, jika pangkalan yang lebih kuat digunakan, seperti LDA, senyawa monocarbonyl juga dapat dialkilasi dalam posisi alfa.
CONTOH 22.7.1: ALFA ALKILASI
Mekanisme
1) Enolate formasi
2) Serangan S N 2
Reaksi dari enolat:
Enolat adalah nukleofil dan dengan demikian dapat bereaksi dengan berbagai electophiles. Tergantung pada jenis elektrofil digunakan kita memiliki kelas yang berbeda reaksi
a. Reaksi aldol:
Sebelumnya, di bawah kondisi dasar yang kita akan bentuk enolat. Berdasarkan pKa dari siapa pun, Anda akan menyadari bahwa pembentukan enolat tidak akan lengkap (hidroksida tidak kuat dasar cukup untuk memastikan deprotonasi lengkap) dan sebagian besar keseimbangan akan terhadap aldehida dan natrium hidroksida. Dengan demikian, hanya sejumlah kecil dari enolat nukleofilik terbentuk. Enolat yang terbentuk akan bereaksi dengan asetaldehida yang molekul yang tidak enolized untuk membentuk alkoksida tersebut. alkoksida ini akan terprotonasi oleh air yang awalnya dibentuk pada langkah pertama. The product of this step is a Hasil dari langkah ini adalah yang mengandung senyawa aldehida (‘sedang dioperasikan pada poros’) serta sebuah hidroksil (‘ol’) kelompok yang nama umum adalah ‘aldol’. Namun nama itu aldol digunakan untuk seluruh kelas reaksi melibatkan suatu enolat dan senyawa karbonil Perhatikan bahwa katalis basa (hidroksida ion) adalah regenerasi di langkah terakhir, jadi ini memang merupakan proses katalitik. (Prof. Santosh Gharpure Prof Santosh Gharpure )
Secara umum, dalam reaksi konsentrasi dasar harus dikontrol. With higher Dengan lebih tinggi dehidrasi produk aldol akan terjadi lebih mudah karena pembentukan konjugasi stabil senyawa karbonil tidak jenuh. penghapusan ini adalah contoh dari Kondensasi aldol Salah satu cara untuk memastikan bahwa produk aldol aldol kondensasi bukan produk dari adalah diperoleh adalah dengan menggunakan kondisi kinetik dibahas sebelumnya untuk melakukan reaksi aldol. Reaksi aldol dapat dikatalisis dalam kondisi asam juga. Namun, dalam kondisi ini biasanya produk kondensasi aldol diperoleh yaitu dehidrasi produk aldol awal berlangsung cepat. Untuk diskusi mekanistik, mari kita pertimbangkan contoh cyclopentanone dengan asam. Dalam media asam, keton tautomerizes nya Para enols jauh kurang nukleofilik daripada enolat Namun, protonasi oksigen karbonil membuat akseptor lebih baik (elektrofil) dari keton unprotonated! (Prof. Santosh Gharpure Prof Santosh Gharpure )
b. Claisen kondensasi atau reaksi:
Generasi enolat dan selanjutnya reaksi tidak terbatas pada keton dan aldehida. Bahkan proton α untuk ester kelompok fungsional asam cukup dan dapat terdeprotonasi dengan dasar untuk membentuk enolat. Enolat ini adalah nukleofilik dan dapat bereaksi dengan berbagai karbonil ester bisa sendiri bertindak sebagai elektrofil. Jadi, etil bila bereaksi dengan natrium etoksida mengarah pada pembentukan β-keto ester, yaitu etil acetoacetate. (Prof. Santosh Gharpure Prof Santosh Gharpure )
Reaksi ini dikenal sebagai reaksi Claisen atau kondensasi Claisen. condensation involves kondensasi melibatkan serangkaian ekuilibria. Semua kesetimbangan adalah bergeser ke arah produk karena stabilitas dari anion dari yang diperoleh sendiri oleh acidifying reaksi. Cara lain untuk menggeser kesetimbangan ke kanan adalah untuk menyaring off alkohol dengan-produk seperti yang terbentuk. Pembentukan enolat pada langkah awal yang terpisah dari reaksi dengan menggunakan basa kuat dan kemudian bereaksi dengan asil klorida juga meningkatkan hasil dari β-keto ester. Ini jauh lebih baik metode banyak terutama untuk mempersiapkan produk campuran ester kondensasi yang biasanya menghasilkan campuran produk. (Prof. Santosh Gharpure Prof Santosh Gharpure )
c. Reaksi Dieckmann
Molekul kondensasi intra diesters menuju pembentukan siklik β-keto ester dikenal sebagai reaksi Dieckmann. Reaksi ini secara mekanis mirip dengan Claisen reaksi dan ini terutama bermanfaat dalam pembentukan lima dan enam beranggota cincin. Catatan: Sangat penting untuk diingat bahwa sama seperti reaksi aldol dan reaksi Claisen Dieckmann adalah reaksi reversibel. (Prof. Santosh Gharpure Prof Santosh Gharpure )
d. Alkilasi Enolat:
Enolat dari aldehida, keton dan ester biasanya mengalami kondensasi reaksi karena mereka juga mengandung sebuah gugus karbonil elektrofilik. Pembentukan enolat anion jauh lebih lancar ketika dua kelompok yang berdekatan dapat menstabilkan muatan negatif. Jenis senyawa yang sering disebut sebagai senyawa metilen aktif – mereka. pKa memiliki nilai yang kurang dibandingkan dengan air dan alcohol. enolat dihasilkan dari senyawa metilen aktif sangat nukleofilik dan dapat mudah alkilasi dengan berbagai alkil halida (elektrofil). Ketika dua atom hidrogen asam yang hadir pada atom karbon yang sama, mono-dan dialkylation keduanya mungkin. Produk yang diperoleh merupakan fungsi sederhana kuantitas reaktan yang digunakan. Dialkylation atau alkilasi berturut-mono dengan dua yang berbeda β-keto pemakan menjalani dekarboksilasi melalui asam β-keto yang sesuai yang sangat meningkatkan utilitas mereka dalam sintesis organik. Produk setelah dekarboksilasi adalah dasarnya mirip dengan yang diperoleh pada alkilasi enolat keton yang sesuai. (Prof. Santosh Gharpure Prof Santosh Gharpure ).
Permasalahan:
1.enolat ester manolat biasanya dibuat dengan mengolah ester itu dengan natrium etoksida. Yang dibuat dengan melarutkan logam natrium dalam etanol tak berair, dimana etanol yang digunakan 95 persen bukan etanol biasa. Dan senyawa yang mempunyai gugus karboksil berposisi beta terhadap senyawa karbonil akan mengalami dekarboksilasi bila dipanasi. Permasalahan saya adalah mengaoa etanol yang digunakan 95 persen dan bagaimana bila produk dari dekarboksilasi tidak di inginkan, tetapi dwi asam nya di ingin kan, bagaimana cara memperoleh nya
2.oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon, dari artikel itu apa hal yang membuat oksigen lebih olektronegatif dan keterkaitan dengan ikatan pada karbon ?
3.. Enol (juga disebut sebagai alkenol) adalah alkena yang mempunyai gugus hidroksil yang melekat pada karbon berikatan rangkap dua. Enol dan senyawa karbonil (seperti keton dan aldehida) sebenarnya adalah isomer; ini dikenal sebagai tautomerisme keto-enol: Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton). Apahal yang menyebabkan tidak stabilnya senyawa yang terbentuk tersebut sehingga ia akan berubah dengan cepat menjadi bentuk keto?

Enol (juga disebut sebagai alkenol) adalah alkena yang mempunyai gugus hidroksil yang melekat pada karbon berikatan rangkap dua. Enol dan senyawa karbonil (seperti keton dan aldehida) sebenarnya adalah isomer; ini dikenal sebagai tautomerisme keto-enol:
BalasHapusEnol.png
Bentuk enol ditunjukkan pada gambar sebelah kanan. Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton) pada gambar sebelah kiri. Hal ini dikarenakan oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon.
Hanya dalam senyawa 1,3-dkarbonil dan 1,3,5-trikarbonil yang memiliki bentuk enol yang stabil. Hal ini disebabkan oleh resonansi dan ikatan hidrogen antarmolekul yang terjadi pada bentuk enol dan tidak mungkin terjadi pada bentuk keto. Oleh karenanya, pada kesetimbangan, lebih dari 99% molekul propanadial (OHCCH2CHO) berbentuk monoenol. Persentase tersebut lebih rendah untuk keton 1,3-aldehida dan diketon. Enol (dan enolat) merupakan zat antara yang penting pada banyak reaksi organik.
Perkataan enol dan alkenol adalah akronim dari alkena (-ena) dan alkohol (-ol).
Ion enolat
Ketika gugus hidroksil (−OH) pada sebuah enol melepaskan ion hidrogen (H+), akan terbentuk enolat yang bermuatan negatif:
Formation of Enolate.PNG
Enolat hanya akan terdapat pada kondisi yang bebas asam Brønsted karena secara umum enolat bersifat sangat basa.
Senyawa 1,3-dikarbonil dan 1,3,5-trikarbonil sedikit asam karena adanya stabilisasi resonansi yang kuat yang terjadi ketika satu atom hidrogen dilepaskan (dari bentuk keto maupun enol). Resonansi enol memiliki analogi yang sama yang digunakan untuk menjelaskan keasaman fenol, yakni terjadi delokalisasi muatan negatif ion enolat ke karbon alfa. Ion-ion enolat ini sangatlah berguna dalam sintesis senyawa alkohol dan karbonil yang rumit. Ia sangat berguna karena karbon-α gugus enolat bersifat nukleofilik.
Pada keton (sejenis karbonil) dengan hidrogen-α yang asam pada kedua karbon di sebelah gugus karbonil, selektivitas deprotonasi dapat dicapai untuk mendapatkan enolat yang kita inginkan. Pada temperatur rendah (-78 °C, yakni dengan penangas es kering), pelarut aprotik, dan basa seperti LDA, proton "kinetik" dapat dilepaskan. Proton "kinetik" adalah proton yang secara sterik lebih mudah dijangkau. Di bawah kondisi termodinamik (temperatur yang lebih hangat, basa lemah, dan pelarut protik), kesetimbangan terjadi antara keton dengan dua enolat yang memungkinkan. Enolat yang difavoritkan diistilahkan sebagai enolat "termodinamik" dan difavoritkan karena ia memiliki aras energi yang lebih rendah dari enolat yang dimungkinkan lainnya.
Nomor 2 Enol (juga disebut sebagai alkenol) adalah alkena yang mempunyai gugus hidroksil yang melekat pada karbon berikatan rangkap dua. Enol dan senyawa karbonil (seperti keton dan aldehida) sebenarnya adalah isomer; ini dikenal sebagai tautomerisme keto-enol: Bentuk enol ditunjukkan pada gambar sebelah kiri. Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton) pada gambar sebelah kanan. Hal ini dikarenakan oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon. .(Wikipedia bahasa Indonesia, ensiklopedia bebas)
BalasHapusHanya dalam senyawa 1,3-dkarbonil dan 1,3,5-trikarbonil yang memiliki bentuk enol yang stabil. Hal ini disebabkan oleh resonansi dan ikatan hidrogen antarmolekul yang terjadi pada bentuk enol dan tidak mungkin terjadi pada bentuk keto. Oleh karenanya, pada kesetimbangan, lebih dari 99% molekul propanadial (OHCCH2CHO) berbentuk monoenol. Persentase tersebut lebih rendah untuk keton 1,3-aldehida dan diketon. Enol (dan enolat) merupakan zat antara yang penting pada banyak reaksi organik.
Saya akan jawab nomor 1.
BalasHapusEnolat ester malonat biasanya dibuat dengan mengolah ester itu dengan natrium etoksida.yang disiapkan dengan melarutkan logam natrium dalam etanol takberair, etanol yang digunakan 95% bukan etanol yang biasa. Hal ini disebabkan karena etanol lebih berperan sebagai pelarut untuk reaksi itu. Kemudian ditambahkan dietil malonat. Ion etoksida merupakan basa yang labih kuat dari pada ion enolat ; oleh karena itu kesetimbangan asam-basa terletak pada sisi anion enolat yang terstabilkan oleh resonansi.
Reaksi alkilasi adalah khas penukar ganti SN2 oleh suatu nukleofil. Metil halida dan alkil halida primer memberikan rendemen terbaik, sementara alkil halida sekunder memberikan rendemen yang lebih rendah karena adanya reaksi eliminasi yang menyaingi.
Jika ester malonat tersubtitusi ataupun tidak, dihidrolisis dalam larutan asam yang panas, terbentuklah suatu dwiasam-β dan dapat menjalani dekarboksilat. (kadang-kadang dekarboksilat baru terjadi pada saat dwiasam ini disuling).
Saya akan mencoba menjawab permasalahan no 2
BalasHapusEnol (juga disebut sebagai alkenol) adalah alkena yang mempunyai gugus hidroksil yang melekat pada karbon berikatan rangkap dua. Enol dan senyawa karbonil (seperti keton dan aldehida) sebenarnya adalah isomer; ini dikenal sebagai tautomerisme keto-enol. Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton). Hal ini dikarenakan oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon.
Generasi enolat keton adalah pada kali menantang karena mereka menimbulkan masalah dalam keton dapat memiliki proton enolizable di kedua sisi karbonil kelompok. Masalahnya tidak begitu banyak bila satu sisi keton tidak memiliki proton enolizable (acetophenone misalnya) atau keton adalah simetris (misalnya 3-pentanone). Masalah sebenarnya adalah dengan keton tidak simetris di mana proton enolizable yang hadir pada Sisi. Untuk reaksi yang sukses, kita harus mengontrol sisi enolat terbentuk. Jika salah satu dari dua proton secara signifikan lebih asam, pembentukan enolat selektif adalah lurus ke depan. Misalnya dalam kasus acetoacetate etil, ada dua jenis enolizable protons. Namun, hanya satu dari dua proton adalah terdeprotonasi pertama . Prinsip ini dapat diperpanjang lebih jauh dimana perbedaan dalam keasaman dari proton. di kedua sisi ini tidak diucapkan. dua enolat yang mungkin seperti yang ditunjukkan. Sekarang enols dan enolat adalah alkena dan karenanya semakin menggantinya, semakin stabil akan. Jadi, ketika kesetimbangan adalah mungkin, enolat lebih stabil akan membentuk. Hal ini dimungkinkan jika tersedia sumber proton, dalam hal ini yang sedikit berlebihan keton itu sendiri dapat bertindak sebagai sumber proton.
Saya akan mencoba menjawab permasalahan yang ke 1 Jika ester malonat tersubtitusi ataupun tidak, dihidrolisis dalam larutan asam yang panas, terbentuklah suatu dwiasam-β dan dapat menjalani dekarboksilat. (kadang-kadang dekarboksilat baru terjadi pada saat dwiasam ini disuling).
BalasHapusKarena oksigen memiliki 2 pasang elektron bebas, dimana PEB ini bersifat elektronegatif, yang menarik awan elektron ke sekitar atom O, sehingga O lebih elektronegatif, sementara Atom C tidak memiliki pasangan elektron bebas.
BalasHapusSaya akan mencoba menjawab permasalahan no 2
BalasHapusEnol (juga disebut sebagai alkenol) adalah alkena yang mempunyai gugus hidroksil yang melekat pada karbon berikatan rangkap dua. Enol dan senyawa karbonil (seperti keton dan aldehida) sebenarnya adalah isomer; ini dikenal sebagai tautomerisme keto-enol. Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton). Hal ini dikarenakan oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon.
Saya akan jawab nomor 1.
BalasHapusEnolat ester malonat biasanya dibuat dengan mengolah ester itu dengan natrium etoksida.yang disiapkan dengan melarutkan logam natrium dalam etanol takberair, etanol yang digunakan 95% bukan etanol yang biasa. Hal ini disebabkan karena etanol lebih berperan sebagai pelarut untuk reaksi itu. Kemudian ditambahkan dietil malonat. Ion etoksida merupakan basa yang labih kuat dari pada ion enolat ; oleh karena itu kesetimbangan asam-basa terletak pada sisi anion enolat yang terstabilkan oleh resonansi.
Saya nenjawab permasalahn no 2Generasi enolat keton adalah pada kali menantang karena mereka menimbulkan masalah dalam keton dapat memiliki proton enolizable di kedua sisi karbonil kelompok. Masalahnya tidak begitu banyak bila satu sisi keton tidak memiliki proton enolizable (acetophenone misalnya) atau keton adalah simetris (misalnya 3-pentanone). Masalah sebenarnya adalah dengan keton tidak simetris di mana proton enolizable yang hadir pada Sisi. Untuk reaksi yang sukses, kita harus mengontrol sisi enolat terbentuk. Jika salah satu dari dua proton secara signifikan lebih asam, pembentukan enolat selektif adalah lurus ke depan. Misalnya dalam kasus acetoacetate etil, ada dua jenis enolizable protons. Namun, hanya satu dari dua proton adalah terdeprotonasi pertama . Prinsip ini dapat diperpanjang lebih jauh dimana perbedaan dalam keasaman dari proton
BalasHapusSaya akan mencoba menjawab permasalahan yang ke 1 Jika ester malonat tersubtitusi ataupun tidak, dihidrolisis dalam larutan asam yang panas, terbentuklah suatu dwiasam-β dan dapat menjalani dekarboksilat. (kadang-kadang dekarboksilat baru terjadi pada saat dwiasam ini disuling).
BalasHapusSaya akan menjawab permasalahan Nomor 2
BalasHapusEnol (juga disebut sebagai alkenol) adalah alkena yang mempunyai gugus hidroksil yang melekat pada karbon berikatan rangkap dua. Enol dan senyawa karbonil (seperti keton dan aldehida) sebenarnya adalah isomer; ini dikenal sebagai tautomerisme keto-enol: Bentuk enol ditunjukkan pada gambar sebelah kiri. Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton) pada gambar sebelah kanan. Hal ini dikarenakan oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon.
Jawaban no 2 Biasanya ia tidak stabil dan berubah dengan cepat menjadi bentuk keto (keton) pada gambar sebelah kanan. Hal ini dikarenakan oksigen lebih elektronegatif daripada karbon, sehingga oksigen membentuk energi ikatan rangkap yang lebih kuat. Ikatan ganda karbon-oksigen (karbonil) lebih kuat dua kali lipat daripada ikatan tunggal karbon-oksigen, namun ikatan ganda karbon-karbon lebih lemah daripada dua ikatan tunggal karbon-karbon.
BalasHapusEnolat hanya akan terdapat pada kondisi yang bebas asam Brønsted karena secara umum enolat bersifat sangat basa. Senyawa 1,3-dikarbonil dan 1,3,5-trikarbonil sedikit asam karena adanya stabilisasi resonansi yang kuat yang terjadi ketika satu atom hidrogen dilepaskan (dari bentuk keto maupun enol). Resonansi enol memiliki analogi yang sama yang digunakan untuk menjelaskan keasaman fenol, yakni terjadi delokalisasi muatan negatif ion enolat ke karbon alfa. Ion-ion enolat ini sangatlah berguna dalam sintesis senyawa alkohol dan karbonil yang rumit. Ia sangat berguna karena karbon-α gugus enolat bersifat nukleofilik.
BalasHapus